Atom
A. PENGERTIAN ATOM
Kata atom berasal dari bahasa Yunani “Atomos”
yang berarti tidak dapat dibagi-bagi. Semua material di dunia ini memiliki
bagian yang kecil-kecil, sehingga jika bagian tersebut dibagi lagi, maka
terdapatlah bagian paling kecil yang tidak dapat dibagi lagi, hal itulah yang
disebtu dengan atom. Atom adalah penyusun materi terkecil dari segala materi
yang ada.
Atom terdiri dari nucleus (inti atom), dan
dikelilingi oleh elektron yang memiliki muatan negative. Pada inti atom,
terdapat proton yang berumatan positif dan neutron yang tidak memiliki muatan
(netral). Atom memiliki diameter sekitar 6-30 nm. Partikel-partikel seperti
proton, neutron dan electron terikat dengan atom oleh karena adanya suatu gaya
elektormagnetik.
Karena gaya elektromagnetik pula, atom dapat bergabung bersama dengan
atom-atom yang lain sehingga membentuk sebuah molekul. Sampai dengan saat ini,
belum ada satupun alat atau teknologi yang dapat melihat atom.
|
|
Beberapa pengertian atom menurut para ahli
yaitu :
§ Leucipus dan Democritus mengatakan bahwa atom adalah bagain
terkecil dari suatu materi yang tidak dapat dibagi lagi menjadi bagian-bagian
tertentu. atom merupakan penyusun segala materi yang ada di dunia ini.
§ John Dalton, mengatakan bahwa atom ialah partikel terkecil daripada suatu zat
yang tidak dapat diuraikan lagi menjadi partikel yang lebih kecil melalui
reaksi kimia biasa.
§ Joseph John Thompson berpendapat bahwa atom merupakan sebuah
bola yang bermuatan positif dan dikelilingi oleh electron seperti roti kismis
§ Ernest Rutherford berpendapat bahwasanya atom ialah atom
merupakan partikel yang terdiri dari neutron dan proton serta dikelilingi oleh
electron.
Terdapat penekanan yang harus dimengerti oleh
setiap orang bahwasanya atom yang tidak dapat dibagi lagi memiliki artian bahwa
atom yang masih dapat dibagi seperti halnya atom oksigen yang dipisah dari
partikel dasar proton, neutron dan elektron bukan merupakan sebuah atom lagi,
melainkan sudah menjadi ion. Artinya, jika atom tersebut dipisahkan dengan zat
atau partikel dasarnya, maka zat tersebut tidak dapat dikatakan atom lagi,
sudah menjadi ion.
B. SEJARAH PENEMUAN ATOM
Sejarah tentang penemuan atom dimulai ketika
John Dalton mengggas sebuah teori tentang atom pad atahun 1803. Kemudian,
terdapat beberapa penelitian yang mendukung teori atom yang dikemukakan oleh
John Dalton, speerti Michael Faraday yang menemukan teori pemecahan molekul
menggunakan elektrolisis pada tahun 1832, dan J.Plucker yang menemukan tabung
katoda pada tahun 1839.
Kemudian diikuti penemuan Dmitri Mendelev
tentang hukum periodic pada tahun 1869, lalu John C.Maxwell pada tahun 1873
yang melakukan penelitian tentang listrik dan medan listrik. Setelah itu
terdapat Sir Willian Crookes yang pada tahun 1870 melalui penelitian
eksperimental menemukan bahwa suatu electron memiliki massa tertentu melalui
percobaan penembakan sinar katoda.
Lalu ada penelitian dari E.Goldstein yang
menemukan proton bermuatan positif. Kemudian G.J Stoney yang berhasil menemukan
partikel penyusun atom yang bermuatan negative yaitu electron. Dan kemudian
penelitian oleh Wilhelm Roentgen yang menemukan X-Ray.
Rutherford kemudian membuat hipotesis
berdasarkan penelitiannya yang mengatakan bahwa terdapat suatu inti atom selain
proton yang menjaga keseimbangan atom. Hipotesis Rutherford ini kemudian
dibuktikan oleh James Chadwik pada tahun 1932 dengan menemukan partikel atom
yang bermuatan netral yang disebut dengan neutron.
C. TEORI – TEORI ATOM
Teori-teori atom selalu mengalami
perkembangan-perkembangan dari waktu ke waktu sesuai dengan penemuan-penemuan
baru yang ditemukan oleh para ahli. Teori tentang atom telah dimulai sejak abad
sebelum masehi. Seorang ahli filsafat Yunani yang bernama Demokritus
berpendapat bahwa sebuah materi bersifat diskontinu, jika materi tersebut
dibelah secara terus-menerus, maka akan didapatkan bagian yang tidak dapat
dibelah lagi. Bagian tersebut dinamakan dengan atom.
1. Teori Atom Dalton
Teori ini disapampaikan oleh John Dalton pad
atahun 1803 M. ia berpendapat berdasarkan dua hukum yang diambil, yaitu hukum
kekekalan massa (Lavoisier) dan hukum susunan tetap (hukum Prouts). Dalam hukum
kekekalan massa, lavosier mengatakan bahwa “massa total zat-zat sebelum reaksi
sama dengan massa total zat-zat hasil reaksi”. Begitu juga dengan hukum susunan
tetap, Prouts berpendapat “perbandingan massa unsur-unsur dalam suatu senyawa
selalu tetap”. Dari kedua hukum itu, maka Dalton menarik kesimpulannya yaitu :
§
Atom merupakan bagian
terkecil materi yang tidak dapat dibagi lagi
§
Atom berbentuk mirip
seperti bola pejal yang snagat kecil, suatu atom memiliki unsur-unsur memiliki
atom-atom yang identikdan berbeda dengan unsur yang berbeda
§
Atom-atom jika
bergabung maka akan membentuk suatu senyawa dengan perbandingan bilangan bulat
dan sederhana.
§
Reaksi kimia merupakan
pemisahan ataupun penggabungan atau penyusunan kembali dari atom-atom, sehingga
atom tidak dapat diciptakan atau dimusnahkan
Teori atom Dalton memunculkan satu kelemahan,
yaitu tidak dapat menjelaskan bagaimana suatu materi dapat menghantarkan
listrik. Bagaimana mungkin sebuah bola pejal menghantarkan listrik, karena
listrik itu dihantarkan oleh electron yang bergerak.
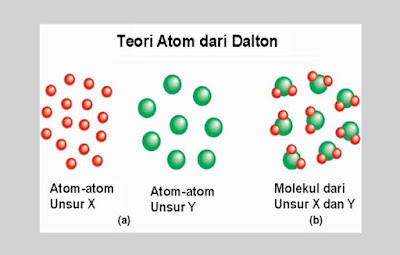 |
|
TEORI ATOM DALTON
|
2. Teori Atom Thomson
Teori ini dikemukakan oleh Joseph John
Thomson. Berawal dari penemuan tabung katode oleh William Crooker, maka
Thompson kemudian meneliti lebih lanjut tentang sinar katode. Ia menemukan
bahwasanya sinar katode merupakan sebuah partikel, karena sinar ini dapat
memutar baling-baling yang diletakkan antara katode dan anode. Dari hasil
inilah ia menyusun kesimpulan bahwa sinar katode merupakan partikel penyusun
atom yang bermuatan negative dan selanjutnya disebut dengan electron.
Lebih lanjut, ia berpendapat bahwa atom
merupakan partikel yang bersifat netral, oleh karena electron bermuatan
negative, maka harus ada suatu partikel lain yang mampu untuk menteralkan hal
tersebut, yaitu partikel positif.
Teori atom Thomson berbunyi “Atom merupakan
partikel yang berbentuk seperti bola pejal dengan muatan positif, dan dialamnya
tersebar muatan negatif”. Bola atom ini dapat diumpakan seperti jambu biji yang
terkelupas kulitnya. Electron di dalam atom persis seperti biji jambu yang
tersebar merata di dalam jambu. Teori Thompson memperbaiki kelemahan dari teori
atom Dalton.
 |
|
TEORI ATOM THOMSON
|
3. Teori Atom Rutherford
Rutherford dibantu oleh dua orang muridnya
yaitu Hans Geigerden dan Erners Masreden melakukan percobaan yang dikenal
dengan hamburan sinar alfa di suatu lempeng emas tipis. Sebelum dilakukan
percobaan ini, terlebih dahulu sudah ditemukan partikel alfa yang bersifat
positif dan bergerak lurus, serta berdaya tembus besar, sehingga dapat menembus
lembaran tipis emas.
Dari hasil penelitian ini, mereka menemukan
bahwasanya ketika ditembakkan sinar alfa ke lempengan tipis emas, maka sebagian
partikel alfa akan diteruskan (walaupun terdapat penyimpangan sudut kurang dari
1`), tetapi dari pengamatan Marsden ditemukan bahwa satu dari 20.000 partikel
alfa akan membelok dengan sudut 90` atau bahkan lebih.
Jadi, dapat ditarik kesimpulan bahwa :
§
Atom bukan berbentuk
bola pejal, karena hampir semua partikel alfa diteruskan
§
Jika lempeng emas itu
dianggap sebagai lapisan atom-atom emas, maka di dalam atom emas didapat
partikel yang sangat kecil bermuatan positif
§
Partikel positif itu
merupakan partikel penyusun inti atom, dan ukuran inti atom lebih kecil 10.000
kali dari ukuran atom
 |
|
TEORI ATOM RUTHERFORD
|
4. Teori Atom Bohr
Pada tahun 1913, seorang pakar fisika bernama
Neils Bohr berusaha untuk memperbaiki teori yang dikemukakan oleh Rutherford.
Ia melakukan sebuah percobaan yang dikenal dengan spectrum atom hydrogen. Dalam
percobaan ini, ia berhasil menemukan gambaran mengenai bagaimana keadaan
electron yang menempati daerah inti atom. Teori Bohr menggabungkan antara teori
mekanika kuantum yang ditemukan oleh Planck dengan teori Rutherford yang
dikemukakan oleh Rutherford. Kemudian, Bohr mengungkapkan empat postulatnya,
yaitu :
§
Hanya ada seperangkat
orbit tertentu yang boleh bagi satu electron dalam satu atom hydrogen. Orbit
ini dikenal dengan orbit stationer (menetap) electron dan merupkaan lintasan
melingkar di sekeliling inti
§
Selama electron berada
di lintasan stationer, energy elektorn akan tetap sehingga tidak ada energy
dalam bentuk radiasi yang dipancarkan atau diserap
§
Elektron dapat
berpindah dari satu lintasan stationer ke lintasan stationer yang lain.
Perpindahan ini juga akan memakan energy sesuai dengan persamaan Plank E2-E1
=hf
§
Lintasan stationer
yang dibolehkan memiliki besaran dengan sifat-sifat tertentu, terutama sifat
yang disebut momentum sudut.
Bohr juga mengungkapkan bahwa
electron-elektron mengelilingi inti pada lintasan-lintasan tertentuyang disebut
kulit electron atau kulit energy. Tingkat energy yang paling rendah adalah
kulit electron yang paling dalam, dan semakin besar nomor kulitnya, maka
semakin besar tingkat energinya.
D. PARTIKEL DASAR ATOM (PROTON, NEUTRON DAN
ELEKTRON)
Seperti yang telah disebutkan di atas, atom
sebenarnya dikelilingi oleh proton yang ebrmuatan positif, neutron yang
bermuatan netral, dan electron yang bermuatan negative. Adanya partikel dasar
ini tidak terlepas dari pengaruh gaya elektromagnetik yang mengikat
partikel-pertikel ini. Pengertian dari masing-masing partikel dasar suatu atom
adalah :
1. Proton
Proton merupakan partikel dasar yang memiliki
muatan positif (+1) dan memiliki diameter hanya 1/3 diameter electron. Akan
tetapi, proton memiliki massa sekitar 1840 kali electron
2. Neutron
Neutron merupakan partikel dasar yang tidak
memiliki muatan (netral), dan memiliki massa yang sama dengan gabungan antara
massa proton dan massa electron
3. Elektron
Merupakan partikel dasar yang memiliki muatan negative
(-1) dan memiliki massa paling ringan diantara partikel lainnya yang hanya
1/1840 kali massa proton atau neutron.
 |
|
PARTIKEL DASAR ATOM
|
E. Partikel-Partikel Atom
1. Partikel Subatom
Walaupun definisi atom menyebutkan bahwa atom
ialah bagian terkecil dari material yang tidak dapat dibagi lagi, dalam ilmu
modern, atom sendiri tersusun atas beberapa partikel subatom. Partikel subatom
ini meliputi proton, elektron dan neutron.
2. Inti Atom
Inti atom terdiri dari proton dan neutron yang
terikat di inti atom oleh suatu gaya elektromagnetik. Proton dan nutron itu
disebut dengan nucleon (penyusun inti). Inti atom memiliki diameter berkisar
10-15 nm. Atom dari unsur kimia yang sama memiliki jumlah proton yang sama
pula. Suatu unsur dapat memiliki variasi jumlah neutron yang disebut dengan
isotop.
3. Awan Elektron
Awan partikel merupakan suatu daerah dalam
sumur potensi dimana tiap-tiap electron menghasilkan sejenis gelombang diam
(gelombang yang tidak bergerak).
F. Sifat-Sifat Atom
1. Sifat Nuklir
Sifat nuklir (radioaktif) hanya dimiliki oleh
unsur-unsur atom yang memiliki nomor atom lebih dari 82. Dari sekitar 339
nuklida yang sudah ditemukan secar alami di bumi, sebanyak 269 diantaranya belum
terpantau secara menyeluruh. Pada unsur kima, 80 dari unsur yang diketahui
memiliki satu atau lebih isotope stabil. Unsur 43, 63, dan semu aunsur yang
memiliki nomor atom lebih dari 82 tidak memiliki isotope stabil. Hal inilah
yang menyebabkan unsur tersebut memiliki sifat radioaktif.
2. Massa Atom
Jumlah keseluruhan dari partikel dasar dalam
suatu atom disebut dengan nomor massa. Massa atom dalam keadaan diam dinilai
dengan menggunakan satuan Dalton. Massa atom dalam unsur yang berbeda memiliki
massa yang bervariasi. Massa tersebut tergantung dari jumlah proton dan neutron
dalam intinya. Semakin besar massa atom, maka semakin kecillah atom tersebut.
3. Nomor Atom
Atom-atom dalam zat yang berbeda memiliki
jumlah proton yang tidak sama dalam intinya. Jumlah proton dalam inti ini disebut dengan nomor
atom.
4. Gaya Atom
Gaya elektromagnetik menjaga elektron yang
bermuatan negatif agar tetap berada orbit sekeliling inti
muatan positif. Terdapat gaya tarik inti yang merupakan gaya paling kuat yang
menjaga proton dan neutron tetap berada dalam inti atom. Gaya inti seratus kali
lebih kuat daripada gaya elektromagnetik.

Komentar
Posting Komentar